
COVID-19 Update para sa Virginia
Agosto 26, 2021
Mahal na Kasamahan:
Salamat sa iyong patuloy na pakikipagtulungan sa pagtugon sa pandemya ng COVID-19 . Mangyaring bisitahin ang website ng Virginia Department of Health (VDH) para sa kasalukuyang gabay sa klinikal at pampublikong kalusugan, epidemiologic data, at iba pang impormasyon. Ang mga update sa mga sumusunod na paksa ay kasama sa sulat na ito:
- Binibigyan ng FDA ng Buong Pag-apruba ang Pfizer-BioNTech COVID-19 Vaccine
- Booster Dose ng mRNA Vaccine para sa Pangkalahatang Populasyon ng Pang-adulto na Magsisimula sa kalagitnaan ng Setyembre
- Coadministration ng COVID-19 at Influenza Vaccine
- Mga Karagdagang Update tungkol sa Respiratory Syncytial Virus
Binibigyan ng FDA ng Buong Pag-apruba ang Pfizer-BioNTech COVID-19 Vaccine
Noong Agosto 23, 2021, ang US Food and Drug Administration (FDA) ay nagbigay ng buong pag-apruba sa unang bakunang COVID-19 , Pfizer-BioNTech COVID-19 na bakuna, para sa mga taong may edad na 16 taong gulang at mas matanda. Ang bakuna ay ibebenta bilang Comirnaty. Ang Emergency Use Authorization (EUA) ng FDA para sa Comirnaty ay patuloy na sasaklawin ang mga indibidwal na may edad na 12 hanggang 15 taong gulang, at ang pagbibigay ng ikatlong dosis sa ilang partikular na immunocompromised na indibidwal na may edad 12 taong gulang at mas matanda. Ang bakunang inaprubahan ng FDA at ang bakunang pinahintulutan ng FDA ay may parehong pormulasyon at maaaring palitan ng paggamit upang magbigay ng serye ng pagbabakuna sa COVID-19 nang hindi nagpapakita ng anumang alalahanin sa kaligtasan o pagiging epektibo. Ang proseso ng pag-iimbak, pangangasiwa, at pag-order para sa bakuna ay hindi nagbago. In-update ng FDA ang mga fact sheet ng Comirnaty at Pfizer-BioNTech nito para sa mga healthcare provider na nangangasiwa ng mga bakuna at para sa mga tatanggap at tagapag-alaga. Magpupulong ang Advisory Committee on Immunization Practices (ACIP) ng CDC sa Agosto 30 upang talakayin ang mga na-update na rekomendasyon para sa Comirnaty.
Ang pag-apruba na ito ay isang mahalagang milestone na dapat magbigay ng katiyakan sa sinumang nag-aalala tungkol sa pagpapabakuna na ang mga bakunang COVID-19 ay gumagana at ligtas. Batay sa mga resulta mula sa klinikal na pagsubok, ang Comirnaty ay 91% epektibo sa pagpigil sa sakit na COVID-19 . Ang FDA ay nagsagawa rin ng mahigpit na post-authorization safety surveillance patungkol sa mga kaso ng myocarditis at pericarditis. Iminumungkahi ng magagamit na panandaliang data na ang karamihan sa mga indibidwal ay ganap na gumaling, gayunpaman ang ilang mga pasyente ay nangangailangan ng suporta sa intensive care. Napag-alaman na ang panganib ay pinakamataas sa mga lalaking may edad na 12 hanggang 17 taong gulang. Ang panganib ng myocarditis sa mga tumatanggap ng bakuna ay natagpuan din na mas mababa kaysa sa panganib ng myocarditis sa panahon at pagkatapos ng aktwal na sakit na COVID-19 .
Sa buong pag-apruba ng FDA, maaari na ngayong gamitin ang Comirnaty sa mga setting na hindi pang-emergency. Bagama't karaniwang pinahihintulutan ng buong pag-apruba ng FDA ang paggamit ng mga produkto na "off-label", ang pangangasiwa ng lahat ng bakuna para sa COVID-19 ay dapat pa ring gawin alinsunod sa mga kinakailangan ng Programa ng Bakuna sa COVID-19 ng CDC at ang mga rekomendasyon ng CDC, ACIP, at FDA. Nalalapat ito sa parehong mga bakunang COVID-19 na inaprubahan ng EUA at FDA. Ang paggamit ng off-label ng anumang bakuna sa COVID-19 ay hindi inirerekomenda at maaaring maglantad sa mga provider sa mga sumusunod na panganib:
- Ang pangangasiwa ng produkto na wala sa label ay maaaring hindi saklaw sa ilalim ng PREP Act o ng deklarasyon ng PREP Act; samakatuwid, ang mga tagapagkaloob ay maaaring walang kaligtasan sa mga paghahabol.
- Ang mga indibidwal na tumatanggap ng isang off-label na dosis ay maaaring hindi karapat-dapat para sa kabayaran sa ilalim ng Countermeasures Injury Compensation Program pagkatapos ng isang posibleng masamang pangyayari.
- Tinukoy ng CDC ang saklaw ng CDC COVID-19 Vaccination Program sa mga tuntunin ng kung paano maaaring gamitin ang mga bakunang ibinigay ng gobyerno ng US sa programa. Ang mga provider na nagbibigay ng mga dosis na wala sa label ay labag sa kasunduan ng provider ng Programa ng CDC na posibleng makaapekto sa kanilang kakayahang manatiling provider sa programa ng CDC.
- Maaaring hindi mabayaran ng mga nagbabayad ang mga bayarin sa pangangasiwa.
Ang mga bakunang Moderna at Johnson & Johnson ay patuloy na ligtas na ibibigay sa pamamagitan ng isang EUA habang sinusuri ng FDA ang data tungkol sa paggamit ng mga ito sa totoong buhay.
Booster Dose ng mRNA Vaccine para sa Pangkalahatang Populasyon na Magsisimula sa kalagitnaan ng Setyembre
Noong Agosto 18, 2021, ang US Department of Health and Human Services (HHS) ay naglabas ng magkasanib na pahayag na nag-aanunsyo sa plano ng Administrasyon para sa COVID-19 booster doses para sa pangkalahatang populasyon na nakatanggap ng kumpletong serye ng mRNA vaccine. Ang booster dose ay tumutukoy sa isang dosis ng bakuna na ibinibigay kapag ang paunang sapat na immune response sa isang pangunahing serye ng bakuna ay malamang na humina sa paglipas ng panahon. Bagama't ang mga bakunang COVID-19 ay patuloy na nagbibigay ng malakas na proteksyon laban sa malubhang karamdaman, pag-ospital, at kamatayan, ipinapakita ng kamakailang ebidensya na ang proteksyon laban sa banayad at katamtamang sakit na COVID-19 ay bumababa sa paglipas ng panahon sa ilang partikular na tao. May pag-aalala na maaaring humina ang proteksyon laban sa pinakamalalang resulta ng COVID-19 sa mga susunod na buwan, lalo na sa mga taong nasa mas mataas na panganib para sa malalang sakit o nabakunahan sa mga naunang yugto ng paglulunsad ng bakuna. Bilang tugon, naglabas ang VDH ng press release at in-update ang Mga FAQ sa Pagbabakuna nito para sa publiko at mga provider ng pangangalagang pangkalusugan.
Batay sa umuusbong na data na ito, ang kasalukuyang iminungkahing plano ay sinumang may edad na 18 taong gulang o mas matanda pa na nakatanggap ng dalawang dosis ng Pfizer-BioNTech (Comirnaty) o Moderna na bakuna ay dapat magplanong makakuha ng booster dose ng hindi bababa sa walong buwan pagkatapos nilang matanggap ang pangalawang dosis simula sa linggo ng Setyembre 20, 2021. Ang mga rekomendasyong ito (kabilang ang timeline) ay maaaring magbago batay sa mga proseso ng pagsusuri ng FDA, ACIP, at CDC. Hindi inirerekomenda ang mga booster sa oras na ito. Ang pagpupulong ng ACIP sa Agosto 30 ay magsasama ng isang talakayan sa mga dosis ng booster. Mangyaring subaybayan ang mga website ng CDC at VDH para sa pinakabagong impormasyon dahil ang impormasyong ito ay maaaring magbago; magpapadala kami ng update sa sandaling mayroon kaming karagdagang impormasyon.
Sa oras ng anunsyo ng HHS, hindi inirerekomenda ang booster dose para sa mga nakatanggap ng Johnson & Johnson vaccine dahil hindi available ang data ng klinikal na pagsubok na kailangan para magawa ang desisyong ito. Noong Agosto 25, iniulat ng Johnson & Johnson na ang mga nabakunahang indibidwal ay may malakas na proteksyon na nagpapatuloy hanggang walong buwan at na ang isang booster dose ay nakabuo ng malaking pagtaas ng spike-binding antibodies sa mga taong may edad na 18–55 taong gulang at sa mga nasa edad na 65 taong gulang o mas matanda na binigyan ng mas mababang dosis ng booster. Ang mga data na ito ay malamang na susuriin ng FDA at CDC upang ipaalam ang mga rekomendasyon sa booster para sa produktong ito.
Bilang paghahanda para sa mga booster dose, kailangan nating tiyakin ang sapat na mga provider ng bakuna para sa COVID-19 para suportahan ang pangangailangan. Kung hindi mo pa nagagawa, mangyaring isaalang-alang ang pagiging isang provider upang suportahan ang iyong komunidad. Para sa karagdagang impormasyon, pakibisita ang Pahina ng Pagpapatala ng Providerng VDH. Bukod pa rito, ang Virginia Vaccine Management and Allocation Exchange (VaxMax) ay nagbibigay ng mga mapagkukunan para sa pag-order, pamamahala, at pamamahagi ng bakuna para sa mga kalahok na tagapagbigay ng pangangalagang pangkalusugan. Kung ang iyong pagsasanay ay nag-aalala noon tungkol sa malaking dami ng minimum na laki ng order, ang Virginia ay mayroon na ngayong Small Shipment Redistribution Program na makakapagbigay ng mas maliliit na dami sa mga tanggapan ng provider. Mangyaring isaalang-alang ang pagpapatala bilang isang tagapagbigay ng bakuna sa COVID-19 ngayon.
Coadministration ng COVID-19 at Influenza Vaccine
Sa papalapit na panahon ng trangkaso (trangkaso), maaaring may mapanghikayat na logistical na mga bentahe sa pag-aalok sa mga pasyente ng COVID-19 at mga bakuna sa trangkaso sa parehong araw. Alinsunod sa klinikal na pagsasaalang-alang ng CDC para sa mga bakunang COVID-19 , maaari mong ligtas na maibigay ang mga bakuna sa COVID-19 at trangkaso (parehong live, attenuated, at non-live na mga bakunang trangkaso) nang walang pagsasaalang-alang sa timing. Kabilang dito ang pangangasiwa ng COVID-19 at mga bakuna sa trangkaso sa parehong araw at kasabay na pangangasiwa sa loob ng 14 na) araw. Kapag nagpapasya kung mag-coadminister ng mga bakuna, mangyaring isaalang-alang ang:
- Kung ang pasyente ay nasa likod o nasa panganib na mahuli sa mga inirerekomendang bakuna
- Ang panganib ng pasyente sa sakit na maiiwasan sa bakuna
- Ang reactogenicity profile ng mga bakuna
- Ang posibilidad na maiwasan ang isang napalampas na pagkakataon upang mabakunahan
Ang pinakamahuhusay na kagawian para sa pagbibigay ng maraming bakuna ay kinabibilangan ng mga sumusunod:
- Lagyan ng label ang bawat syringe ng pangalan at ang dosis (halaga) ng bakuna, numero ng lot, ang mga inisyal ng naghahanda, at ang eksaktong oras ng lampas sa paggamit, kung naaangkop.
- Paghiwalayin ang mga lugar ng pag-iniksyon ng 1 pulgada o higit pa, kung maaari.
- Pangasiwaan ang mga bakuna at bakuna para sa COVID-19 na maaaring mas malamang na magdulot ng lokal na reaksyon (ibig sabihin, mga adjuvanted influenza vaccine) sa iba't ibang paa, kung maaari.
Ang pagbabakuna sa trangkaso ay magbabawas sa pasanin ng mga sakit sa trangkaso, pagka-ospital at pagkamatay sa sistema ng pangangalagang pangkalusugan at makakatulong na makatipid ng mga mapagkukunan ng pangangalagang pangkalusugan para sa COVID-19 at iba pang mga kondisyon.
Mga Karagdagang Update tungkol sa Respiratory Syncytial Virus
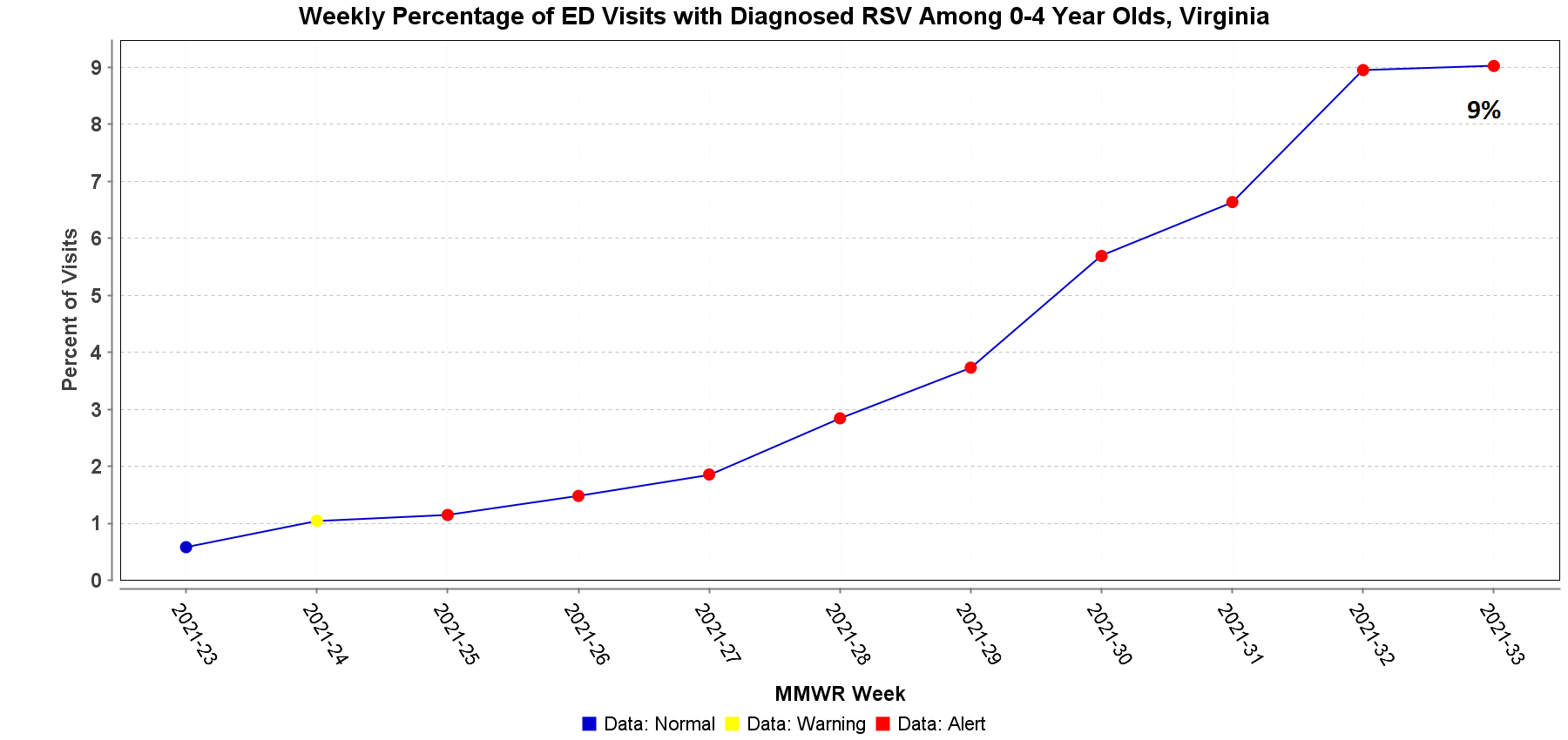
Sa aming Agosto 6, 2021 Dear Colleague letter, nagbigay kami ng impormasyon tungkol sa respiratory syncytial virus (RSV) prophylaxis. Simula noon, in-update ng American Academy of Pediatrics (AAP) ang pansamantalang gabay nito para sa palivizumab prophylaxis. Lubos na sinusuportahan ng AAP ang mga provider na isaalang-alang ang paggamit ng palivizumab sa mga pasyente na magiging mga kandidato ayon sa kasalukuyang mga rekomendasyon sa pagiging kwalipikado. Ina-update ng binagong patnubay ang timing kung kailan ibibigay ang palivizumab upang matugunan ang binagong seasonality ng RSV ngayong taon. Nalalapat ang rekomendasyon ng AAP sa mga rehiyong may mataas na rate ng sirkulasyon ng RSV, na naaayon sa karaniwang taglagas-taglamig na panahon. Ang VDH ay nakakakita ng pagtaas sa bilang ng mga naiulat na paglaganap ng RSV. Ang bilang ng mga paglaganap ng RSV na iniulat ay isa noong Hunyo, tatlo noong Hulyo, at labing-isa noong Agosto sa ngayon. Sa linggo ng Agosto 15–21, 9% ng mga pagbisita sa emergency department sa mga batang may edad na 0 hanggang 4 na taon sa Virginia ay na-diagnose na may RSV.
Gaya ng dati, taos-puso akong nagpapasalamat sa iyong patuloy na pakikipagtulungan sa mga mapanghamong panahong ito. Kung mayroon kang mga tanong tungkol sa COVID-19, mangyaring makipag-ugnayan sa iyong lokal na departamento ng kalusugan.
Taos-puso,
M. Norman Oliver, MD, MA
Komisyoner ng Kalusugan ng Estado
